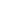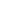創新器械每前進一步都離不開政策的配套助力,此次國家層面再度明確,鼓勵創新醫療器械發展,創新器械的市場化道路周期正在縮短。
01
DRG/DIP動態調整,鼓勵新技術、新器械進醫保
近日,國家醫保局發布《國家醫療保障局關于政協十四屆全國委員會第一次會議第02870號(社會管理類217號)提案答復的函》。

其中提出,“推動建立基本醫保、商業健康保險等的多層次醫療保障體系,鼓勵將新技術、新藥品、新器械納入保障范圍,激發藥品企業創新研發動力。在DRG/DIP等醫保支付方式改革中,充分考慮新技術、新藥品、新器械的應用,科學測算病種分值,并建立動態調整機制。”
政策層面,國家已不止一次在支付環節為創新器械留出綠色通道,一些地方上的推進也受到了國家層面的肯定。
今年3月,國家醫保局在《對十三屆全國人大五次會議第3298號建議的答復》中就曾點名支持北京在CHS-DRG付費政策中有關特殊藥品、器械、高值耗材、新技術的創新機制。
《答復》中提到:“北京市對于符合一定條件的藥品、醫療器械及診療項目,納入CHS-DRG付費除外支付管理;河北邯鄲明確了付費異常高值和異常低值的病組可按項目付費,確定特殊治療、特殊用藥,高值耗材的清單,可以不納入DRG分組,確保全覆蓋。”
而最新的答復函也從國家層面再次明確了對于新技術、新器械的鼓勵支持。
02
多地發文,創新器械迎來政策東風
近年來,轟轟烈烈的耗材帶量采購通過采購環節的以量換價,給器械市場帶來顯著影響。同時,DRG/DIP改革也在重塑醫院運營理念和方式,進而影響市場的產品選擇,產品過關、性價比高的耗材越來越受到歡迎。
在兩大政策之下,耗材市場的格局也在悄然轉變,許多細分賽道已經歷了過去多年未曾有多的大調整。縱向來看,改革率先對技術成熟、規模較大的重點品類形成影響,伴隨相關政策的深入推進,降價等因素也開始影響諸多創新企業及產品。
在改革過程中,支持創新再度被提起。今年7月,國家衛健委等多部門發布的《關于印發深化醫藥衛生體制改革2023年下半年重點工作任務的通知》中明確,推進醫藥領域改革和創新發展。
據觀察,一段時間以來,多地發文,從醫保支付等方面加大對創新藥械的支持力度。
12月8日,浙江醫保局發布了《浙江省創新醫藥技術醫保支付激勵管理辦法(試行)(征求意見稿)》,其中明確,符合條件的創新醫藥技術經申報和認定后,可納入醫保支付激勵范圍。
7月,上海提出要加快創新藥械臨床應用。調整優化醫療機構考核機制,醫院不得以用藥目錄數量、“藥/耗占比”等原因限制創新藥械入院。加大創新藥械醫保支付支持。在DRG/DIP支付方面對創新藥械予以傾斜,提高新技術應用病例支付標準,新技術應用高倍率病例不設控制比例,成規模新技術應用可獨立成組。穩步擴大本市醫療服務項目和醫用耗材醫保支付范圍,優先覆蓋創新藥械。
此前,北京市決定試行CHS-DRG付費新藥新技術除外支付管理辦法。
這些舉措都為創新技術、創新藥械開辟出一條通道,有利于創新產品進入市場,服務醫患。不過,真正的創新和微創新之間的界限微妙,醫學的高壁壘性導致一些“灰色操作”極其隱蔽。因此,國家和地方層面都對“何為創新”做出了具體規定,真正能改善臨床效果、具有明顯技術創新的產品將獲益。
今年10月,國家醫保局對“關于從價格和醫保報銷政策加快新技術價格項目審核,納入醫保報銷問題”進行回復。
答復函中提出,調研中發現,有的新增價格項目訴求,是因為價格項目跟技術細節綁定過深,臨床實踐稍有變化可能就無法匹配現有項目,醫療機構需通過申報新增價格項目方可進臨床使用收費。有的新增價格項目申報質量不高,將現行價格項目進行拆分、組合、改頭換面,導致不少省份每年收到醫療機構申報新增價格項目數千項,其中重復及低質量申報占比較高,影響了新增價格項目審核的工作效率。

地方上也有相應要求。如浙江省規定創新醫療服務項目(含醫用材料)須同時滿足:三年內本省批準設立的新增醫療服務項目(省本級已經設立的新技術項目除外);在操作途徑、操作方法、解剖部位、適用范圍等方面有明顯的技術創新;臨床效果較臨床主流使用的醫療服務項目有較大提升等條件。
此外,對于創新產品的扶持也有時間限制。浙江醫保局上述《征求意見稿》中明確了“激勵期限原則上為3年”。北京市醫保局也規定,“除外范圍內的藥品、醫療器械及診療項目在未來三年(指含獲批除外支付年度及之后的兩個自然年度)有效”。
整體來看,在新的行業環境下,以往耗材的超長利潤紅利期被大幅壓縮,市場將更加充分的檢驗和篩選真正有價值的產品,對于企業各項核心競爭力的挑戰也在升級。
(文章來源于互聯網)




 全部商品分類
全部商品分類